この記事のトピックは水蒸気 分 圧について書いています。 水蒸気 分 圧について学んでいる場合は、この水上ガスの収集練習問題 – 化学ガス法記事で水蒸気 分 圧についてcsmetrics.orgを明確にしましょう。
目次
水上ガスの収集練習問題 – 化学ガス法新しいアップデートの水蒸気 分 圧に関連するビデオの概要
このウェブサイトComputerScienceMetricsでは、水蒸気 分 圧以外の情報を追加して、より価値のあるデータを提供できます。 Webサイトcsmetrics.orgでは、ユーザーのために毎日新しい情報を継続的に更新します、 最も詳細な知識をあなたにもたらしたいと思っています。 ユーザーがインターネット上の知識をできるだけ早く更新できる。
水蒸気 分 圧に関連するいくつかの説明
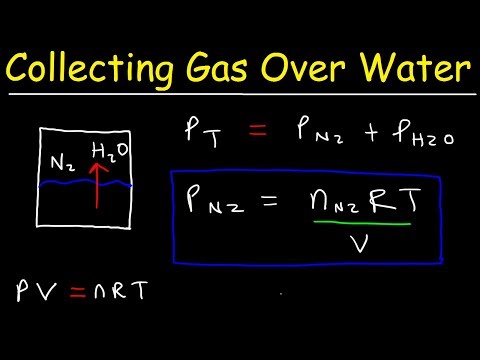
この化学のビデオ チュートリアルでは、水上でガスを集める練習問題を解決する方法を説明します。 温度によって変化する水の蒸気圧を考慮する必要があります。 新しい化学ビデオ プレイリスト: プレミアム ビデオへのアクセス: Facebook:
水蒸気 分 圧の内容に関連する画像
視聴している水上ガスの収集練習問題 – 化学ガス法に関する情報を発見することに加えて、csmetrics.orgが継続的に公開している他の情報を検索できます。
水蒸気 分 圧に関連する提案
#水上ガスの収集練習問題 #化学ガス法。
collecting gas over water practice problems,collecting gas over water problems,collecting gas over water,chemistry,gas laws,problems,practice problems。
水上ガスの収集練習問題 – 化学ガス法。
水蒸気 分 圧。
水蒸気 分 圧の知識により、Computer Science Metricsがあなたのために更新されることが、あなたがより多くの新しい情報と知識を持っているのを助けることを願っています。。 ComputerScienceMetricsによる水蒸気 分 圧に関する記事をご覧いただきありがとうございます。

My friend, you're a life saver.
I’m confused, why do we have to convert from torr to atm if both pressures were given in torr…
hello JG do you have an email adress i can contact you with i have these tutorial questions that i would appreciate if you would look at they are so nuanced but simple in thier solutions id like if you could explain some of the theory behind solving them
quick question…….out of all the R constants, why is it the one with atm you decide to use as your R
thank you
7:33 I think the kelvin calculation there is wrong as 22 degrees celsius is 295.15
Wow thank you! Typical engineering first-year chemistry problem, I thought I would never find this!
One of the biggest donation
Get this man to 3 million he is so close!!!
This is a really long question, so bear with me.
I don't understand why we can use the total volume of the sample to calculate moles of nitrogen collected.
– if we change the pressure (by finding the partial pressure of nitrogen) shouldn't that also change either the volume or temp? If we removed the water vapor from the container but kept the pressure of the nitrogen constant (at its partial pressure which would then be the total pressure), wouldn't that change the volume?
Is it somehow tied to kinetic-molecular theory?
Thanks for these videos! I'm teaching high school chemistry but my degree is in biology and my students are really smart and always ask questions like that (above) so whenever I feel like my understanding is tenuous I come here!
OMG THANK YOU!! I had no clue how to solve these problems! also I have my chem test in six hours and I still need to go to sleep!! 😀🔫 wish me luck 3/26/21
goat
i love you
MEA?
What if there was also a pressure of air in the flask along with water?? so confused…
Thanks for this video. For anyone who’s watching, please try to attempt each problem before he finishes it and when you get the questions right you will feel good. However, Once you finish the video without trying and re watch it to do so, it won’t work as well…
Do you round up the answers with respect to the sig figs?
Great video. Very helpful. Thanks!
Thank you!
It really helps thank you but in the last question, can i find the moles of potassium chlorate from the water vapor instead of O2 ?
At around 10:36, why is the partial pressure for O2 calculated? Just wondering why it's O2 instead of some other substance regarding the finding of partial pressure.
Anyone else grinding these out for the ap exam
Your the best
I love you
If I know you earlier, I won't be so stress about AP Chemistry
THANK YOU!